╝¬└¹Ą┬ę¬Ū¾╚ĪŽ¹╚Ą┬╬„Ēf╣┬ā║╦Ä┘YĖ±
üĒį┤Ż║Clindata ū„š▀Ż║ ĢrķgŻ║2020-3-26 ķåūxŻ║

Gilead Sciences Statement on Request to Rescind Remdesivir orphan Drug Designation Gilead has submitted a request to the U.S. Food and Drug Administration to rescind the orphan drug designation it was granted for the investigational antiviral remdesivir for the treatment of COVID-19 and is waiving all benefits that accompany the designation. Gilead is confident that it can maintain an expedited timeline in seeking regulatory review of remdesivir, without the orphan drug designation. Recent engagement with regulatory agencies has demonstrated that submissions and review relating to remdesivir for the treatment of COVID-19 are being expedited.
In early March, Gilead sought and was subsequently granted an orphan drug designation for the remdesivir as a potential treatment for COVID-19. orphan drug designation is granted by the FDA in situations where the disease affects fewer than 200,000 patients in the United States.
Among the benefits of orphan drug designation, this status results in a waiver of the requirement to provide a pediatric study plan prior to the submission of a New Drug Application ©C a process that can to take up to 210 days to review.
Gilead recognizes the urgent public health needs posed by the COVID-19 pandemic. The company is working to advance the development of remdesivir as quickly as possible, and will provide updates as they become available.
╚šŪ░Ż¼╝¬└¹Ą┬┐ŲīW╣½╦ŠĄ─į┌čą┐╣▓ĪČŠ»¤Ę©╚Ą┬╬„ĒfŻ©remdesivirŻ®½@Ą├├└ć°FDA╩┌ėĶĄ─╣┬ā║╦Ä┘YĖ±Ż©orphan drug designationŻ®Ż¼▀mæ¬░Y×ķą┬╣┌▓ĪČŠ▓ĪŻ©COVID-19Ż®ĪŻ▀@ę╗Ž¹Žóę²Ų┴╦▓╗╔┘ĀÄūhŻ¼ėąą®śIĮń╚╦╩┐ō·ą─╣┬ā║╦Ä┘YĖ±┐╔─▄Ģ■ė░Ēæ╚Ą┬╬„ĒfĄ─┐╔╝░ąįĪŻĮ±╚šŻ¼╝¬└¹Ą┬┐ŲīWŻ©Gilead SciencesŻ®╣½╦Š░l▓╝┬Ģ├„Ż¼ą¹▓╝ęčĮøŽ“├└ć°FDA╠ß│÷╔ĻšłŻ¼ę¬Ū¾ FDA╩š╗ž╩┌ėĶ╚Ą┬╬„ĒfĄ─╣┬ā║╦Ä┘YĖ±Ż¼▓óŪęĘ┼Śē┼c╣┬ā║╦Ä┘YĖ±ŽÓĻPĄ─╦∙ėąā×╗▌ÖÓęµĪŻ
╝¬└¹Ą┬┐ŲīW▒Ē╩ŠŻ¼ėąą┼ą─╝┤╩╣į┌ø]ėą╣┬ā║╦Ä┘YĖ±Ą─ŪķørŽ┬Ż¼╚į─▄▒Ż│ų╚Ą┬╬„Ēf▒O╣▄īÅįu▀^│╠Ą─╝ė╦┘═Ļ│╔ĪŻĮ³╚šįō╣½╦Š┼c▒O╣▄ÖCśŗĄ─Į╗┴„▒Ē├„Ż¼┼c╚Ą┬╬„Ēfų╬»¤COVID-19ŽÓĻPĄ─╔Ļšł║═īÅįuČ╝īó▒╗╝ė┐ņĪŻ
į┌3į┬│§Ż¼╝¬└¹Ą┬┐ŲīWŽ“FDAīżŪ¾½@Ą├╣┬ā║╦Ä┘YĖ±Ż¼ķ_░l╚Ą┬╬„Ēfū„×ķų╬»¤COVID-19Ą─Øōį┌»¤Ę©ĪŻ╣┬ā║╦Ä┘YĖ±╩ŪFDA╣─äŅķ_░lų╬»¤║▒ęŖ▓ĪĄ─┤ļ╩®ų«ę╗Ż¼×ķßt╦Ä╣½╦Šķ_░lį┌čą»¤Ę©╠ß╣®ČÓĘNā×╗▌š■▓▀ĪŻŲõųąę╗ĒŚā×╗▌╩Ū┐╔ęį├Ō╚źį┌ą┬╦Ä╔ĻšłŪ░▀fĮ╗ā║┐Ų蹊┐ėŗäØŻ©pediatric study planŻ®ĪŻ▀@ę╗▀^│╠Ą─īÅįuĢrķg┐╔─▄ķL▀_210╠ņĪŻ
╝¬└¹Ą┬┐ŲīW╣½╦Šį┌┬Ģ├„ųą▒Ē╩ŠŻ║Ī░ ╝¬└¹Ą┬šJūRĄĮCOVID-19┤¾┴„ąą▓ĪĦüĒĄ─Šo╝▒╣½╣▓ąl╔·ąĶŪ¾ĪŻ╣½╦Šš²į┌ęį▒M┐╔─▄┐ņĄ─╦┘Č╚═Ų▀M╚Ą┬╬„ĒfĄ─ķ_░lĪŻĪ▒
╚Ą┬╬„Ēf╩Ū╩▄ĄĮÅVĘ║ĻPūóĄ─┐╣▓ĪČŠį┌čą»¤Ę©Ż¼╦³─┐Ū░į┌6ĒŚ┼R┤▓įć“×ųąĮė╩▄Öz“ׯ¼ų╬»¤▓╗═¼ŅÉą═Ą─COVID-19╗╝š▀ĪŻŲõųąŻ¼į┌ųąć°▀MąąĄ─ā╔ĒŚ┼R┤▓įć“×ėą═¹į┌4į┬Ę▌½@Ą├ĮY╣¹ĪŻ
3į┬23╚šŻ¼FDA╣┘ŠWöĄō■Äņ’@╩ŠŻ¼FDA╩┌ėĶ╝¬└¹Ą┬┐ŲīWŻ©Gilead SciencesŻ®╣½╦Šķ_░lĄ─į┌čą┐╣▓ĪČŠ»¤Ę©╚Ą┬╬„ĒfŻ©remdesivirŻ®╣┬ā║╦Ä┘YĖ±Ż©Orphan Drug DesignationŻ®Ż¼Ųõ▀mæ¬░Y×ķ╣┌ĀŅ▓ĪČŠ╝▓▓Ī2019Ż©COVID-19Ż®ĪŻ
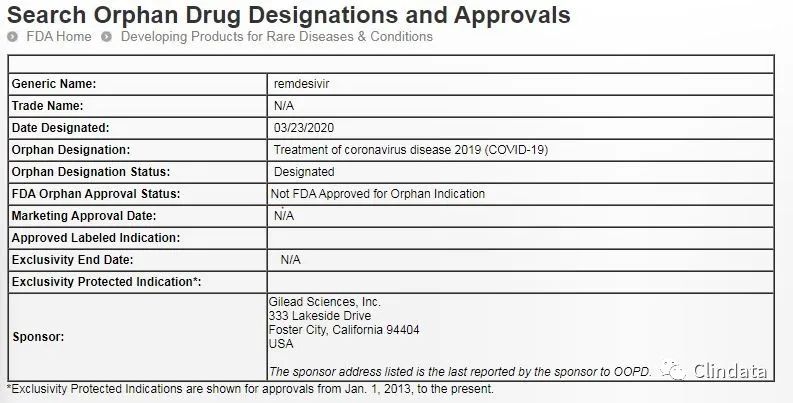
FDAĄ─╣┬ā║╦Ä┘YĖ±šJČ©ĒŚ─┐ų╝į┌┤┘▀Mų╬»¤║▒ęŖ╝▓▓Ī╗“ĀŅørĄ─╦Ä╬’╗“╔·╬’ųŲŲĘĄ─ķ_░lĪŻ║▒ęŖ╝▓▓ĪĄ─Č©┴x╩Ūį┌├└ć°╗╝▓Ī╚╦öĄąĪė┌20╚f╚╦ĪŻ½@Ą├╣┬ā║╦Ä┘YĖ±Ą─į┌čą»¤Ę©─▄ē“½@Ą├ę╗ŽĄ┴ą┤┘▀M╦Ä╬’ķ_░lĄ─ā×╗▌Ż¼Ųõųąųžę¬Ą─ę╗Śl╩Ū╚ń╣¹įō»¤Ę©Ą─╣┬ā║╦Ä▀mæ¬░Y½@Ą├┼·£╩Ż¼įō╦Ä╬’┐╔ęįį┌▀@ę╗▀mæ¬░YĘĮ├µŽĒėą7─Ļ╩ął÷¬Üš╝Ų┌Ż©exclusivityŻ®ĪŻęŌ╬Čų°╚ń╣¹FDA┼·£╩╚Ą┬╬„Ēfė├ė┌ų╬»¤COVID-19Ż¼7─Ļā╚Ųõ╦³ßt╦Ä╣½╦Šķ_░lĄ─Ę┬ųŲ╦Ä▓╗─▄į┌├└ć°╔Ž╩ąĪŻ│²┤╦ęį═ŌŻ¼į┌╦Ä╬’ķ_░l▀^│╠ųąŻ¼čą░l╣½╦Š▀Ć─▄ē“½@Ą├┼c║ŽĖ±┼R┤▓£yįćŽÓĻPĄ─ČÉ䚥ų├ŌŻ¼ęį╝░▀fĮ╗ą┬╦Ä╔ĻšłĢr╠žČ©┘Mė├Ą─£p├ŌĄ╚Ųõ╦³ā×╗▌ĪŻ
╝¬└¹Ą┬┐ŲīW╣½╦Šķ_░lĄ─╚Ą┬╬„ĒfĮ³üĒ│╔×ķ┤¾╝ęĻPūóĄ─¤ß³c╦Ä╬’ĪŻ╦³╩Ūę╗┐Ņ┐╣▓ĪČŠ»¤Ę©Ż¼Ųõū„ė├ÖCųŲ×ķęųųŲRNAę└┘ćąįRNAŠ█║Ž├ĖĄ─╗ŅąįŻ¼Å─Č°ęųųŲRNA▓ĪČŠĄ─į÷ų│ĪŻ─┐Ū░Ż¼╝¬└¹Ą┬╣½╦Šš²į┌▀Mš╣6ĒŚ┼R┤▓įć“ׯ¼Öz“×╚Ą┬╬„Ēfų╬»¤▓╗═¼ŅÉą═Ą─COVID-19╗╝š▀Ą─»¤ą¦ĪŻŲõųąŻ¼į┌ųąć°▀MąąĄ─ā╔ĒŚ┼R┤▓įć“×ėą═¹į┌4į┬½@Ą├ĮY╣¹ĪŻ
×ķ┴╦ØMūŃ┐╔─▄│÷¼FĄ─╬┤üĒąĶŪ¾Ż¼įō╣½╦ŠęčĮøöU┤¾╚Ą┬╬„ĒfĄ─╔·«a─▄┴”Ż¼▓óŪęīó╔·«aā╔ĘN╚Ą┬╬„ĒfĄ─┼õĘĮŻ©ę║¾w║═ā÷Ė╔Ż®ĪŻū“╚šŻ¼įō╣½╦Š▒Ē╩ŠŻ¼─┐Ū░š²į┌īó╠ß╣®éĆ╚╦═¼Ūķ╩╣ė├Ż©compassionate useŻ®Šo╝▒═©Ą└▀^Č╔ĄĮöUš╣╩╣ė├ĒŚ─┐Ż©expanded access programsŻ®Ż¼▀@ĘNĘĮĘ©īó╝ė╦┘ųž░Y╗╝š▀½@Ą├╚Ą┬╬„ĒfĄ─ÖCĢ■Ż¼▓ó─▄ē“╩š╝»╦∙ėąģó┼c╗╝š▀Ą─öĄō■ĪŻ▀@ą®ĒŚ─┐─┐Ū░š²į┌┼c╚½Ū“Ė„ć°▒O╣▄ÖCśŗ┬ō║Ž┐ņ╦┘ķ_░lĪŻ
3į┬18╚šŻ¼▒Ŗ╦∙Ų┌┤²Ą─┬ÕŲź─ŪĒf-└¹═ą─ŪĒfų╬»¤ą┬╣┌┼R┤▓įć“×ĮY╣¹Ż¼į┌ĪČą┬ėóĖ±╠mßtīWļsųŠĪĘ╔Ž░l▓╝Ż¼ĮY╣¹ūī╚╦╩¦═¹Ż¼į┌ųž░Y╗╝š▀ųąŻ¼┼c│ŻęÄų╬»¤ŽÓ▒╚Ż¼čąŠ┐╬┤─▄ė^▓ņĄĮ┬ÕŲź─ŪĒf-└¹═ą─ŪĒfų╬»¤Ą─ėąą¦ąįĪŻ
2į┬│§Ż¼ų╝į┌įu╣└┬ÕŲź─ŪĒf-└¹═ą─ŪĒfų╬»¤ą┬╣┌Ą─┼R┤▓įć“ׯ¼į┌╬õØhĮŃy╠Čßtį║ķ_š╣ĪŻ
įć“×╣▓╝{╚ļ199├¹ą┬╣┌▓ĪČŠ┤_į\╗╝š▀Ż¼ļSÖCĮė╩▄│ŻęÄų╬»¤ĮMŻ¼║═│ŻęÄų╬»¤╝ėŲź─ŪĒf-└¹═ą─ŪĒfų╬»¤ĪŻ┼R┤▓Ė─╔Ų║═▓ĪČŠŪÕ│²Ūķør╩Ūā╔éĆĻPµIųĖś╦Ż¼ĮY╣¹’@╩ŠŻ║
┼R┤▓░YĀŅĖ─╔ŲŻ║ā╔ĮM╗╝š▀│÷¼F┼R┤▓ĀŅørĖ─╔Ųųą╬╗ĢrķgŽÓ═¼Ż¼Š∙×ķ16╠ņĪŻ┬ÕŲź─ŪĒf-└¹═ą─ŪĒfĮM┼c│ŻęÄų╬»¤ĮM╗╝š▀Ą─’LļU▒╚×ķ1.31Ż©95% ų├ą┼Č╚Ż¼0.95-1.80Ż®Ż¼╬┤─▄▒Ē¼F│÷’@ų°▓Ņ«ÉĪŻ
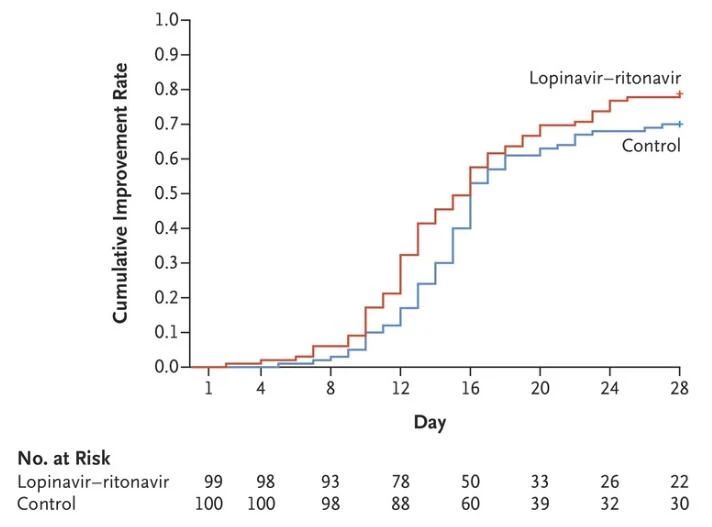
▓ĪČŠŪÕ│²ŪķørŻ║┼c│ŻęÄų╬»¤ĮMŽÓ▒╚Ż¼┬ÕŲź─ŪĒf-└¹═ą─ŪĒfø]ėąĮĄĄ═▓ĪČŠRNA▌d┴┐Ż¼ę▓¤oĘ©┐sČ╠Öz│÷▓ĪČŠRNAĄ─ĢrķgĪŻįć“×ĮY╩°ĢrŻ©Ą┌28╠ņŻ®Ż¼┬ÕŲź─ŪĒf-└¹═ą─ŪĒfĮMėą40.7%Ą─╗╝š▀╚į┐╔Öz│÷ą┬╣┌▓ĪČŠRNAŻ¼║═│ŻęÄų╬»¤ĮM¤o▓Ņ«ÉĪŻ
┤╦═ŌŻ¼į┌░▓╚½ąįĘĮ├µŻ¼┬ÕŲź─ŪĒf-└¹═ą─ŪĒfĮM╗╝š▀│÷¼F┴╦4Ų╬Ė─cĄ└ć└ųž▓╗┴╝╩┬╝■Ż©░³└©É║ą─ĪóćI═┬║═Ė╣×aŻ®Ż¼Č°│ŻęÄų╬»¤ĮM╬┤░l╔·╬Ė─cĄ└ć└ųž▓╗┴╝╩┬╝■ĪŻ
ŠC║ŽĮY╣¹╩ŪŻ║║═│ŻęÄų╬»¤ŽÓ▒╚Ż¼┬ÕŲź─ŪĒf-└¹═ą─ŪĒfų╬»¤Ż¼į┌Ė─╔Ų┼R┤▓░YĀŅ║═ŪÕ│²▓ĪČŠĘĮ├µ▓ó¤oā×ä▌Ż¼▀Ćėą┐╔─▄į÷╝ė▓╗┴╝Ę┤æ¬ĪŻ
ĻPė┌┬ÕŲź─ŪĒf-└¹═ą─ŪĒf
┬ÕŲź─ŪĒf-└¹═ą─ŪĒfŻ¼╔╠ŲĘ├¹┐╦┴”ųźŻ¼2000─Ļ½@FDA┼·£╩╔Ž╩ąŻ¼ė├ė┌ų╬»¤░¼ū╠▓ĪĪŻ
į┌┤╦Ū░Ą─SARSę▀Ūķ║═MERSę▀Ūķ▒¼░l║¾Ż¼┬ÕŲź─ŪĒf-└¹═ą─ŪĒfČ╝ū„×ķėąØō┴”Ą─ų╬»¤╦Ä╬’Ż¼Ą½į┌┼R┤▓įć“×ųąŻ¼Č╝ø]ėą«a╔·┤_ĶÅĄ─ėąą¦ūCō■ĪŻ
ßśī”COVID-19Ż¼┬ÕŲź─ŪĒf-└¹═ą─ŪĒf▀Ć╩Ū¤oą¦ĪŻ¼Fį┌Ż¼ų╗─▄Ų┌┤²╚Ą┬╬„Ēf┼R┤▓öĄō■┴╦ĪŻ
ĻPė┌Č■Ų┌šł³cō¶Ż║äéäéŻĪ├└ć°Remdesivir (╚Ą┬╬„Ēf)ų╬»¤COVID-19▀mæ¬ąįįOėŗüĒ┴╦ŻĪČ■Ų┌öM╚ļĮM394└²▓╔ė├7ĘųŅÉėąą“ūā┴┐ū„×ķų„ę¬ĮK³c
ęįŽ┬╩Ū╚²Ų┌┼R┤▓įć“×ĘĮ░ĖŻ║
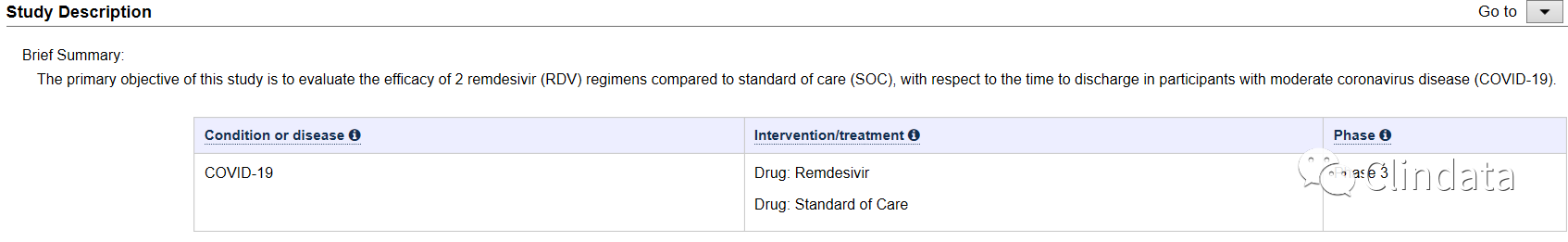
| Arm | Intervention/treatment |
|---|---|
| Experimental: Remdesivir (RDV), 5 Days
Participants will receive continued standard of care therapy together with RDV 200 mg on Day 1 followed by RDV 100 mg on Days 2, 3, 4, and 5. |
Drug: Remdesivir
Administered as an intravenous infusion Other Name: GS-5734™ Drug: Standard of Care Standard of care therapy per local written policies or guidelines |
| Experimental: Remdesivir, 10 Days
Participants will receive continued standard of care therapy together with RDV 200 mg on Day 1 followed by RDV 100 mg on Days 2, 3, 4, 5, 6, 7, 8, 9, and 10. |
Drug: Remdesivir
Administered as an intravenous infusion Other Name: GS-5734™ Drug: Standard of Care Standard of care therapy per local written policies or guidelines |
| Active Comparator: Continued SOC Therapy
Participants will receive continued standard of care therapy. |
Drug: Standard of Care
Standard of care therapy per local written policies or guidelines |
Outcome Measures
Primary Outcome Measures :
-
Proportion of Participants Discharged by Day 14 [ Time Frame: First dose date or randomization date up to 14 days ]
Secondary Outcome Measures :
-
Proportion of Participants With Treatment Emergent Adverse Events Leading to Study Drug Discontinuation [ Time Frame: First dose date up to 10 days ]
Eligibility Criteria
| Ages Eligible for Study: | 18 Years and older (Adult, Older Adult) |
| Sexes Eligible for Study: | All |
| Accepts Healthy Volunteers: | No |
Criteria
Key Inclusion Criteria:
-
Willing and able to provide written informed consent prior to performing study procedures
-
Severe Acute Respiratory Syndrome Coronavirus (SARS-CoV)-2 infection confirmed by polymerase chain reaction (PCR) test Ī▄ 4 days before randomization
-
Currently hospitalized with fever defined as temperature Ī▌ 36.6 ĪŃC armpit, Ī▌ 37.2 ĪŃC oral, or Ī▌ 37.8 ĪŃC rectal
-
Peripheral capillary oxygen saturation (SpO2) > 94% on room air at screening
-
Radiographic evidence of pulmonary infiltrates
Key Exclusion Criteria:
-
Participation in any other clinical trial of an experimental treatment for COVID-19
-
Concurrent treatment with other agents with actual or possible direct acting antiviral activity against SARS-CoV-2 is prohibited < 24 hours prior to study drug dosing
-
Requiring mechanical ventilation at screening
-
Alanine Aminotransferase (ALT) or aspartate aminotransferase (AST) > 5 X upper limit of normal (ULN)
-
Creatinine clearance < 50 mL/min
Note: Other protocol defined Inclusion/Exclusion criteria may apply.
Brief Summary:
The primary objective of this study is to evaluate the efficacy of 2 remdesivir (RDV) regimens compared to standard of care (SOC), with respect to the time to discharge in participants with moderate coronavirus disease (COVID-19).
| Condition or disease | Intervention/treatment | Phase |
|---|---|---|
| COVID-19 | Drug: Remdesivir Drug: Standard of Care | Phase 3 |
Study Design
| Study Type : | Interventional (Clinical Trial) |
| EstimatedEnrollment : | 600 participants |
| Allocation: | Randomized |
| Intervention Model: | Parallel Assignment |
| Masking: | None (Open Label) |
| Primary Purpose: | Treatment |
| Official Title: | A Phase 3 Randomized Study to Evaluate the Safety and Antiviral Activity of Remdesivir (GS-5734™) in Participants With Moderate COVID-19 Compared to Standard of Care Treatment |
| Estimated Study Start Date : | March 2020 |
| Estimated Primary Completion Date : | May 2020 |
| Estimated Study Completion Date : | May 2020 |
Arms and Interventions
| Arm | Intervention/treatment |
|---|---|
| Experimental: Remdesivir (RDV), 5 Days
Participants will receive continued standard of care therapy together with RDV 200 mg on Day 1 followed by RDV 100 mg on Days 2, 3, 4, and 5. |
Drug: Remdesivir
Administered as an intravenous infusion Other Name: GS-5734™ Drug: Standard of Care Standard of care therapy per local written policies or guidelines |
| Experimental: Remdesivir, 10 Days
Participants will receive continued standard of care therapy together with RDV 200 mg on Day 1 followed by RDV 100 mg on Days 2, 3, 4, 5, 6, 7, 8, 9, and 10. |
Drug: Remdesivir
Administered as an intravenous infusion Other Name: GS-5734™ Drug: Standard of Care Standard of care therapy per local written policies or guidelines |
| Active Comparator: Continued SOC Therapy
Participants will receive continued standard of care therapy. |
Drug: Standard of Care
Standard of care therapy per local written policies or guidelines |
Outcome Measures
Primary Outcome Measures :
-
Proportion of Participants Discharged by Day 14 [ Time Frame: First dose date or randomization date up to 14 days ]
Secondary Outcome Measures :
-
Proportion of Participants With Treatment Emergent Adverse Events Leading to Study Drug Discontinuation [ Time Frame: First dose date up to 10 days ]
Eligibility Criteria
| Ages Eligible for Study: | 18 Years and older (Adult, Older Adult) |
| Sexes Eligible for Study: | All |
| Accepts Healthy Volunteers: | No |
Criteria
Key Inclusion Criteria:
-
Willing and able to provide written informed consent prior to performing study procedures
-
Severe Acute Respiratory Syndrome Coronavirus (SARS-CoV)-2 infection confirmed by polymerase chain reaction (PCR) test Ī▄ 4 days before randomization
-
Currently hospitalized with fever defined as temperature Ī▌ 36.6 ĪŃC armpit, Ī▌ 37.2 ĪŃC oral, or Ī▌ 37.8 ĪŃC rectal
-
Peripheral capillary oxygen saturation (SpO2) > 94% on room air at screening
-
Radiographic evidence of pulmonary infiltrates
Key Exclusion Criteria:
-
Participation in any other clinical trial of an experimental treatment for COVID-19
-
Concurrent treatment with other agents with actual or possible direct acting antiviral activity against SARS-CoV-2 is prohibited < 24 hours prior to study drug dosing
-
Requiring mechanical ventilation at screening
-
Alanine Aminotransferase (ALT) or aspartate aminotransferase (AST) > 5 X upper limit of normal (ULN)
-
Creatinine clearance < 50 mL/min
Note: Other protocol defined Inclusion/Exclusion criteria may apply.
╔ŽŲ¬Ż║
Ž┬Ų¬Ż║





 Ė╩╣½ŠW░▓éõ 62010002000454╠¢
Ė╩╣½ŠW░▓éõ 62010002000454╠¢